السبائك و أنواع السبائك وصناعة السبائك
ما المقصود بالسبيكة؟
تعريف السبيكة:هي ما يتكون من فلزين أو أكثر مثل ( الحديد و الكروم ) أو (الحديد و المنجنيز ) أو ( الحديد و الفانديوم ) أو ( الحديد و النيكل ) و يمكن ان تتكون من فلز و عناصر لا فلزية مثل الكربون .
طرق تحضير السبائك
1- تحضر السبائك عادة بصهر الفلزات مع بعضها و ترك المنصهر ليبرد تدريجيا .
2- الترسيب الكهربى : بالترسيب الكهربى لفلزين أو أكثر فى نفس الوقت .
مثال على الترسيب الكهربى :تغطية المقابض الحديدية بالنحاس الاصفر ( نحاس + خارصين ) و ذلك بترسيبه كهربيا على هذه المقابض من محلول يحتوى على أيونات النحاس و الخارصين .
أنواع السبائك
- يتكون اى فلز نقى من شبكة بلورية من ذرات الفلز مرصوصة رصا محكما بينها مسافات بينية .
- عند الطرق عليها يمكن أن تتحرك طبقة من ذرات الفلز فوق طبقة أخرى .

أولاً : السبائك البينية
يتم فيها إدخال ذرات فلز أقل حجما فى المسافات البينية للشبكة البللورية للفلز الاصلى ( أكبر حجما ) ◄◄ مما يعوق إنزلاق الطبقات فتزيد صلابة الفلز بالإضافة الى تأثر بعض خواصه الفيزيائية الأخرى مثل قابلية الطرق و السحب و درجات الانصهار و التوصيل الكهربى و الخواص المغناطيسية .
مثال :سبيكة الحديد و الكربون ( الحديد الصلب )
ثانياً : السبائك الاستبدالية
يتم فيها إستبدال بعض ذرات الفلز الأصلى بذرات فلز أخر بشروط:
مميزات العناصر المكونة لها ( شروطها ) :
- لهما نفس القطر .
- لهما نفس الشكل البلورى .
- لهما نفس الخواص الكيميائية .
أمثلة :
- سبيكة ( الحديد و الكروم ) فى الصلب الذى لا يصدأ .
- سبيكة ( الذهب و النحاس ) .
- سبيكة الحديد و النيكل .
-
ثالثاً : السبائك البينفلزية
- فيها تتحد العناصر المكونة للسبيكة اتحاداً كيميائيا فتتكون مركبات كيميائية .
-
مميزات العناصر المكونة لها (شروطها ) :
- مركبات صلبة .
- لا تخضع صيغتها الكيميائية لقوانين التكافؤ .
- تتكون من فلزات لا تقع فى مجموعة واحدة فى الجدول الدورى .
أمثلة :
-
سبيكة ( الالومنيوم – النيكل ) و ( الألومنيوم – النحاس ) و المعروفتان باسم الديور الومين
-
سبيكة ( الرصاص – الذهب ) Au2Pb
-
سبيكة السيمنتيت Fe3C
خواص الحديد
-
أولاً : الخواص الفيزيائية
تعتمد الخواص الفيزيائية للحديد على نقائه و طبيعة الشوائب به ، و يمكن إنتاج عدد هائل من انواع الصلب و سبائك الحديد لها صفات عديدة تجعلها صالحة لإستخدامات كثيرة .
و فيما يلى أهم الخواص للحديد النقى :
- الحديد النقى ليس له أى اهمية صناعية ( علل ) فهو لين نسبياً و ليس شديد الصلابة .
- قابل للسحب و الطرق لذلك يسهل تشكيله .
- له خواص مغناطيسية .
- ينصهر عند درجة 1538oC و كثافته 78 g/cm3
ثانياً : الخواص الكيميائية
- بخلاف العناصر التى قبله فى السلسلة الإنتقالية الأولى لا يعطى الحديد حالة تأكسد تدل على خروج جميع إلكترونات المستويين الفرعيين(4s , 3d ) و هى ثـمان إلكترونات .
- جميع حالات التأكسد الأعلى من (+3) ليست ذات أهمية .
- له حالة تأكسد ( +2) تقابل خروج إلكترونى المستوى الفرعى 4s .
- حالة التأكسد ( +3 ) تقابل 3d نصف ممتلئ ( حالة ثبات ) .
أهم تفاعلات الحديد
1) تأثير الهواء أو الأكسجين
يتفاعل الحديد المسخن لدرجة الاحمرار مع الهواء أو الأكسجين ويتكون أكسيد حديد مغناطيسى
3Fe(s) + 2O2(g) → Fe3O4 (s)
2) أثر بخار الماء
يتفاعل الحديد المسخن لدرجة الاحمرار عند 500oC مع بخار الماء ويتكون أكسيد حديد مغناطيسى ويتصاعد غاز الهيدروجين.
3Fe(s) + 4H2O (g) → Fe3O4 (s)+ 4H2(g)
3) مع اللافلزات

4) مع الأحماض
أولاً: الأحماض المخففة :ٍ
|
علل : يذوب الحديد فى الأحماض المخففه ليعطى أملاح حديد II و لا يتكون أملاح حديد III ؟ ج : لأن الهيدروجين الناتج عامل مختزل يختزلها . |
تفاعل الحديد مع حمض الهيدروكلوريك المخفف :
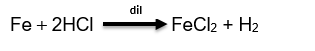
- تفاعل الحديد مع حمض الكبريتيك المخفف :
-

تفاعل الحديد مع حمض الكبريتيك المخفف ثانياً :الأحماض المركزة
- تفاعل الحديد مع حمض الكبريتيك المركز الساخن:-
- يعطى كبريتات حديد II و كبريتات حديد III وثانى أكسيد كبريت وماء
-

تفاعل الحديد مع حمض الكبريتيك المخفف - ثالثا :مع حمض النيتريك المركز
يحدث خمول للحديد لتكون طبقة رقيقة من الأكسيد على سطح الفلز تحميه من استمرار التفاعل يمكن ازلتها بالحك او اذابتها فى حمض الهيدروكلوريك المخفف .
-
: كيف تميز بين حمض الكبريتيك المخفف وحمض الكبريتيك المركز ؟؟.
ج : بإضافة الحديد الى كل منهما مع تقريب شظيه مشتعلة فإذا :
- حدث فرقعة ولهب ازرق يكون الحمض المخفف بسبب تصاعد غاز الهيدروجين .
- لم يحدث شئ يكون الحمض المركز .
