الطلاء بالكهرباء وتحضير الألومنيوم وتنقية المعادن(النحاس)
بعض التطبيقات الهامة للتحليل الكهربى
يتناول هذا الدرس بعض التطبيقات الهامة للتحليل الكهربى مثل الطلاء بالكهرباء وتحضير الألومنيوم وتنقية المعادن(تنقية النحاس)
الطلاء بالكهرباء
عملية تكوين طبقة رقيقة من فلز معين على سطح فلز آخر لإعطائه مظهرا جميلا ولامعاً أو لحمايته من التآكل

الغرض من طلاء المعادن :
1- إعطاء الأدوات المعدنية مظهراً لامعاً .
2- إعطاء المعادن قيمة أكبر بتغطيتها بمعدن نفيس مثل الذهب أو الفضة .
3- حفظ المعادن من التآكل .
مثال : طلاء إبريق بطبقة من الفضة
الطريقة :
1- ينظف سطح الإبريق تماماً ويغمس فى محلول إلكتروليتى يحتوى على أيونات الفضة
( نترات الفضة )
2- يوصل الإبريق بالقطب السالب للبطارية ويصبح مهبط ( كاثود )
3- نضع فى المحلول عمود من فلز الفضة يوصل بالقطب الموجب للبطارية ويصبح مصعد ( آنود ) وبذلك نحصل على خلية إلكتروليتية .
تحضير الألومنيوم
الخام المستخدم :
البوكسيت ( Al2O3 ) المذاب فى مصهور الكريوليت
( Na3 Al F6 ) المحتوى على قليل من الفلوسبار ( CaF2 )

ملحوظة
الكريوليت مادة مذيبة للبوكسيت ، الفلوسبار ( مادة صهارة تخفض
ملحوظة
الكريوليت مادة مذيبة للبوكسيت ، الفلوسبار ( مادة صهارة تخفض درجة انصهار المخلوط من
( C 2045°إلى C 950° )
– حديثاً يستبدل الكريوليت بمخلوط من أملاح فلوريدات كل من الألومنيوم والصوديوم والكالسيوم ، حيث أن هذا المخلوط يعطى مع البوكسيت مصهور يتميز بانخفاض درجة انصهاره ، وكذلك انخفاض كثافته ، حيث أن انخفاض كثافة المصهور يسهل فصل الألومنيوم المنصهر الذى يكون راسباً فى قاع خلية التحليل الكهربى
تركيب خلية التحليل :
1- المهبط ( الكاثود ): هو جسم إناء الخلية المصنوع من الحديد ، ومبطن بطبقة من الكربون ( الجرافيت )
2- المصعد ( الآنود ) : عبارة عن اسطوانات من الجرافيت .
طريقة العمل :
– عند مرور التيار الكهربى بين قطبى الخلية يحدث تفاعل أكسدة واختزال :
عند الكاثود : 2Al+3 + 6e– → 2Al
عند الآنود : –3O-2 → 1.5 O2 + 6e
ويكون التفاعل الكلى :
3O-2 2Al+3 → 1.5O2(g) + 2Al
يتفاعل الأكسجين المتصاعد مع أقطاب الكربون مكوناً غاز أول وثانى أكسيد الكربون
1.5O2+2C → CO + CO2
لذلك يلزم تغيير أقطاب الكربون من آن لآخر بسبب تآكلها
– يسحب الألومنيوم من الخلية من فتحة خاصة بذلك .
لذلك يلزم تغيير أقطاب الكربون من آن لآخر بسبب تآكلها
– يسحب الألومنيوم من الخلية من فتحة خاصة بذلك .
تنقيـة المعادن
المعادن المحضرة صناعياً تكون درجة نقاوتها أقل من الدرجة المطلوبة لبعض الاستخدامات المعينة فتقلل من كفاءتها
مثال : النحاس الذى نقاوته 99 % والذى يحتوى على شوائب من الحديد والخارصين والذهب والفضة ، التى تقلل من قابلية النحاس للتوصيل الكهربى وتقلل من جودته
– لذلك تستخدم طريقة التحليل الكهربى لتنقية النحاس الذى يراد استعماله فى صناعة الأسلاك الكهربية .
الغرض منها : تنقية المعادن من الشوائب
تنقيـة النحاس
تركيب خلية التحليل :
1- الآنود ( القطب الموجب ) هو فلز النحاس Cu° غير النقى
2- الكاثود( القطب السالب ) عبارة عن سلك أو رقائق من النحاس النقى
3- محلول التوصيل الكهربى عبارة عن محلول مائى من كبريتات النحاس التى تتفكك جزيئاتها فى الماء
SO4-2 والكبريتات Cu+2إلى أيونات النحاس
CuSO4(aq) → Cu+2 + SO4-2

الخطوات :
1- عند إمرار التيار الكهربى من البطارية الخارجية عند جهد يزيد قليلاً عن الجهد القياسى لنصف خلية النحاس ، تتجه الأيونات نحو الأقطاب المخالفة فى الشحنة
3- عند الآنود يذوب النحاس ( يتأكسد ) ويتحول إلى أيونات نحاس Cu+2 تنتشر فى المحلول
4- تترسب أيونات النحاس من المحلول فى صورة نحاس نقى مرة أخرى عند الكاثود
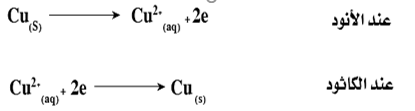
– الشوائب الموجودة فى مادة المصعد( الآنود ) بعضها يذوب ( يتأكسد ) فى المحلول مثل الحديد والخارصين ولا تترسب على الكاثود لصعوبة اختزالها بالنسبة لأيونات النحاس .
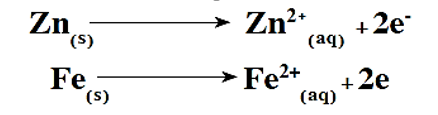
– أما الشوائب الأخرى مثل الذهب والفضة إذا وجدت فى مادة الآنود فلا تتأكسد ( لا تذوب ) عند جهد تأكسد النحاس وتتساقط أسفل الآنود وتزال من قاع الخلية
– أمكن بهذه الطريقة الحصول على نحاس درجة نقاوته 99.5 % ، كما أمكن فصل بعض المعادن النفيسة مثل الذهب والفضة من خامات النحاس
تدريب
علل:
1- تطلى خلاطات المياه بالكروم والذهب
لحمايتها من التأكل واكسابها شكلاً جمالياً
2-الكتلة المكافئة للصوديوم تساوى كتلته المولية بينما الكتلة المكافئةالجرامية للماغنسيوم تساوى نصف كتلته المولية
لأنه يلزم لترسيب 1 mol من الصوديوم 1 mol من الإلكترونات بينما يلزم لترسيب 1 mol من الماغنسيوم يلزم 2 mol من الإلكترونات
3-يفضل الاستعاضة عن الكريوليت بمخلوط من فلوريدات ( الألومنيوم والصوديوم والكالسيوم ) فى خلية التحليل الكهربى للبوكسيت
لأن هذا المخلوط يعطى مع البوكسيت مصهور يتميز بانخفاض درجة انصهاره ، وكذلك انخفاض كثافته
4- يلزم تغيير أقطاب الجرافيت فى خلية التحليل الكهربى للبوكسيت من آن لآخر
بسبب تفاعلها مع الأكسجين المتكون فيتكون أول وثانى أكسيد الكربون
5- تتساقط ذرات الذهب والفضة أسفل الآنود فى خلية تنقية فلز النحاس بالتحليل الكهربى
لأنها لا تتأكسد عند الآنود لصغر جهود أكسدتها مقارنة بالحديد والنحاس والخارصين
6- لا تترسب ذرات الحديد والخارصين على الكاثود فى خلية تنقية فلز النحاس بالتحليل الكهربى
لصعوبة اختزال أيوناتها بسبب صغر جهود اختزالها مقارنة بجهد اختزال النحاس
